肝炎实验动物模型
6.1自身免疫性肝病动物模型应用成年豚鼠,在无菌条件下,先使豚鼠肝素化,而后用生理盐水经门脉进行肝脏灌流,剪断动、静脉以驱除肝内存血。除去胆囊、胆管及其他组织。将肝剪成小块,再以生理盐水浸洗直至无血色。取湿重10g的肝组织,加100ml生理盐水,在组织匀浆器中以8000转/分转4min制成10%的肝悬液。按1:1的比例加入弗氏佐剂,用小注射器往返抽注制成乳剂。成年豚鼠用上述乳剂腹腔注射2ml及4个足垫皮内注射0.1ml。每周一次,免疫1个月后,肝脏内可发生水肿样变性、嗜酸性坏死、肉芽肿样病灶、胆管上皮增生及淋巴细胞和嗜伊红细胞浸润。
实验动物模型复制构建,英瀚斯生物是专业的。
6.2转基因乙肝模型【操作步骤】构建人乙型肝炎病毒(HBV)全基因或部分基因质粒,通过转基因技术将乙型肝炎病毒插入到小鼠基因组上,形成能产生乙型肝炎的小鼠品系。【结果分析】乙型肝炎病毒转基因小鼠,有病毒复制,可用于研究HBV基因结构和功能、基因表达的调控、HBV的复制等。乙型肝炎病毒转基因小鼠会发生免疫逃避,不产生和人类乙型肝炎相近的病理表现。目前,中国医学科学院、***医学科学院、上海复旦大学和广州空军医院拥有乙型肝炎病毒转基因小鼠。 实验动物模型制作周期多久?新疆小鼠实验动物模型怎么样
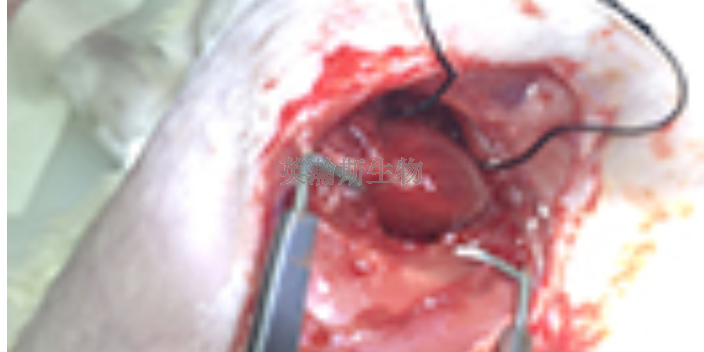
理想的人类疾病实验动物模型应该是标准化的,可重复再现的。应尽量选择标准化实验动物,也应在标准化动物实验设施内完成,要均一性。复制的动物模型来应该力求可真实地反映人类疾病,即可特异地、可靠地反映某种疾病或某种机能、代谢、结构变化,应具备该种疾病的主要症状和体征,经化验或X光照片、心电图、病理切片等证实。若易自发地出现某些相应病变的动物,就不应加以选用,易产生与复制疾病相混淆的疾病者也不宜选用。供医学实验研究用的动物模型,在复制时,应尽量考虑到今后临床应用和便于控制其疾病的发展,以利于研究的开展。如雌ji素能终止大鼠和小鼠的早期妊娠,但不能终止人的妊娠。因此,选用雌ji素复制大鼠和小鼠终止早期妊娠的模型是不适用的。有的动物对某致病因子特别敏感,极易死亡,也不适用。如狗腹腔注射粪便滤液引起腹膜炎很快死亡(80% 24小时内死亡),来不及做实验医疗观察,而且粪便剂量及细菌菌株不好控制,因此不能准确重复实验结果。黑龙江构建实验动物模型怎么选择大鼠实验动物模型都有哪些?
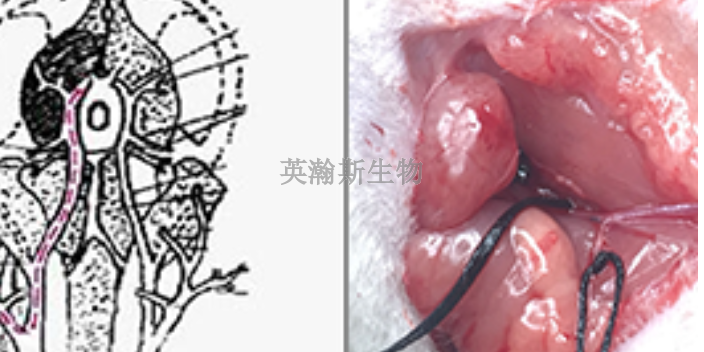
关于老年痴呆(阿尔茨海默症)的实验动物模型,英瀚斯生物小编总结。AD由于其疾病本身的复杂性,单一造模存在很大弊端,越来越多的研究趋向于复合造模,目前为止,尚无对复合造模效果的比较研究,由于AD的发病机制不够明确,且猜想靶点和致病因素较多,世界范围内目前未发现能够全方面的模拟人类衰老、疾病和并发症的动物模型。但多数学者认为,采用复合方法造模能在很大程度上表现出更为接近AD特征的模型动物,为痴呆的研究提出了更深入的探索方向。迄今为止没有公认的AD动物模型,研究者只能从药物和疾病本身的特征出发,选择匹配度较高的模型用于研究。一般而言,基础研究的药效评价多数依赖于动物指标,所以模型的选择、模型成功与否、能否精细造模以符合疾病特征等是实验过程中我们需要慎重考虑的问题。而新的动物模型需要能准确地预测实验医疗的功效,从而使药物从实验室到病床的转化成为可能。
实验动物模型之炎症性肠病模型。炎症性肠病是基因、免疫、饮食、环境等多种因素参与的一种慢性疾病,随着现代的生活方式的改变,炎症性肠病已经越来越普遍,炎症性肠病简单的可以分为溃疡性结肠炎(UC)和克罗恩病(CD)两种,其致残率和致死率呈现持续的上升趋势。为了研究相对应的医疗药物,迄今为止科学研究者已经开发出60多种动物模型,主要可以分为以下几类:化学诱导模型(急性炎症模型,慢性炎症模型),转基因动物模型,自发性疾病模型。英瀚斯生物专业做实验外包服务,一站式医学科研平台。实验动物模型公司靠谱吗?
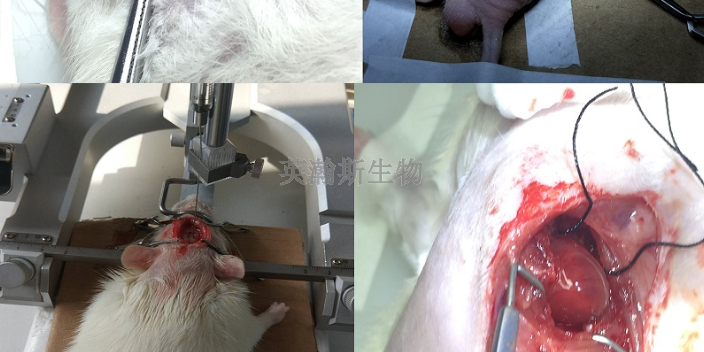
卵巢早衰模型的建立
临床的卵巢早衰(POF)是指卵巢功能提前减退,常见为女性在40岁以前出现闭经,以闭经,不育,雌***缺乏以及**水平升高为特征的一种疾病。在人群中发病率为1%~3%,在继发性闭经中占2%~10%,诊断以至少半年或半年以上闭经多次发生,排除其他原因为基础,卵巢早衰是妇科分泌领域的常见病。
英瀚斯生物可承接各种生殖系统相关实验动物模型。
一.实验方法:
方法一:顺铂诱导大鼠卵巢早衰模型取雌性8周龄SD大鼠,适应性饲养7d。腹腔注射顺铂2mg/kg,连续注射7d。
方法二:环磷酰酸诱导大鼠卵巢早衰模型取雌性8周龄SD大鼠,适应性饲养7d。使用环磷酰酸给予腹腔注射,***次剂量为50mg/kg,以后8mg/kg连续注射14d。 实验动物模型在哪买?四川专业实验动物模型怎么样
英瀚斯生物,承接小鼠实验动物模型。新疆小鼠实验动物模型怎么样
新一代AD(阿尔兹海默症)实验动物模型。尽管APP-Tg小鼠在过去十几年中范围广的被用于开发新的AD医疗策略,但这种小鼠的基因表型和AD患者的还是不同。而且上述的转基因动物模型在Aβ的生成、tau蛋白的过度磷酸化、神经纤维缠结等病理特征上和AD患者的差异也很大,无法理想地模拟AD患者。为了克服这些不希望出现的问题,研究人员构建了带有Swedish(KM670/671NL)、Beyreuther/Iberian(I716F)和Arctic突变等APP基因敲入(APP-KI)小鼠。APP-KI小鼠在没有过度表达APP的情况下生成Aβ42。随着年龄的增长,APP-KI小鼠大脑皮层和海马区出现过多的Aβ沉积。另一方面,与其他AD模型一样,该模型没有tau病理、NFTs、神经退行性变或大量神经元丢失可用于研究临床前AD。由于基因组编辑的新的进展,尤其是CRISPR/Cas技术,未来对转基因动物模型进行改良也值得期待。新疆小鼠实验动物模型怎么样