HE染色不管怎么操作,始终无法染色或淡染答:这种情况一般因为组织固定时采用了酸性甲醛;或者组织在甲醛中浸泡时间太长;或者久置的甲醛变性分解为甲酸。补救:防患于未然,要么使用新鲜的中性甲醛固定,要么在存放的甲醛中加一点碳酸钠中和甲酸。对于已经固定的组织可考虑再次固定;对于已经制出的片子,染色前采用5%重铬酸钾溶液浸泡半小时以上,然后自来水漂洗5min,可改善染色。也可以将切片放入3%硫酸铁铵溶液中,补充染色媒介,增强苏木素与组织的亲和力(苏木素染色必须要媒介才能染上,单纯的苏木素与组织的亲和力很弱)。关于HE染色,你不知道的实验技巧。安徽值得信赖的HE染色公司
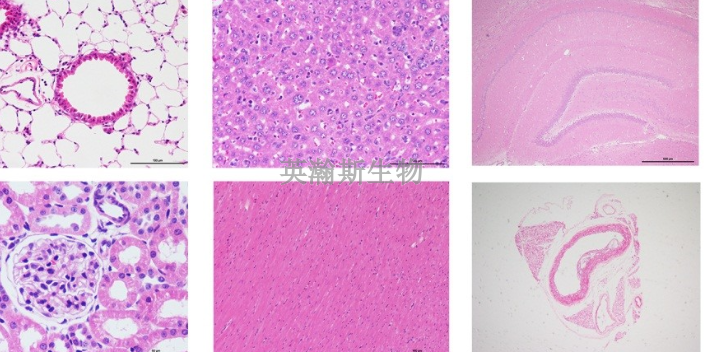
HE染色是苏木精 — 伊红染色法 ( hematoxylin-eosin staining ) ,简称HE染色法 ,石蜡切片技术里常用的染色法之一 。苏木精染液为碱性 ,主要使细胞核内的染色质与胞质内的核酸着紫蓝色 ;伊红为酸性染料 ,主要使细胞质和细胞外基质中的成分着红色 。HE染色法是组织学、胚胎学、病理学教学与科研中**基本、使用*****的技术方法。由于组织或细胞的不同成分对苏木精的亲和力不同及染色性质不一样。经苏木精染色后,细胞核及钙盐粘液等呈蓝色,可用盐酸酒精分化和弱碱性溶液显蓝,如处理适宜,可使细胞核着清楚的深蓝色,胞浆等其它成分脱色。再利用胞浆染料伊红染胞浆,使胞浆的各种不同成分又呈现出深浅不同的粉红色。故各种组织或细胞成分与病变的一般形态结构特点均可显示出来。辽宁专业的HE染色服务HE染色 ,石蜡切片技术里常用的染色法之一。

HE染色伊红着色淡分析及应对原因:(1)伊红染液的pH值可能大于5;(2)蓝化液残留过多;(3)切片太薄;(4)切片经伊红染色后在乙醇脱水时间过长。对策:检查伊红染液的pH值,如果必要的话,用乙酸将其调节在4~5之间,从而使伊红染色彩艳丽。确保每次蓝化步骤完成后,使用的弱碱性溶液被充分洗去,玻片上没有残留的弱碱性溶液。检查切片的厚度。脱水时不要让切片在低浓度乙醇停留时间过长,因为含水多的低浓度乙醇会将伊红的颜色分化掉。
HE染色实验步骤:(1)样品制备:对于贴壁生长细胞,胰酶消化,调整细胞浓度约1×105/ml,滴加于盖玻片上(置于6孔板中),培养相应时间后,取出细胞爬片,用PBS洗涤3次。(2)样品固定:95%乙醇固定20min,PBS洗涤2次,每次1min。(3)染核:苏木素染液染色2-3min,自来水洗涤。(4)分色:镜下观察,若细胞核染色过深,用1%盐酸酒精溶液分色数秒,自来水洗涤。(5)染胞质:浸入伊红染液染色1min,自来水洗涤。(6)吹干或自然晾干细胞爬片后,中性树胶封片。若细胞用4%多聚甲醛固定,则染色时间相应延长,苏木素染色12-15min,伊红5min即可冰冻组织切片的HE染色。
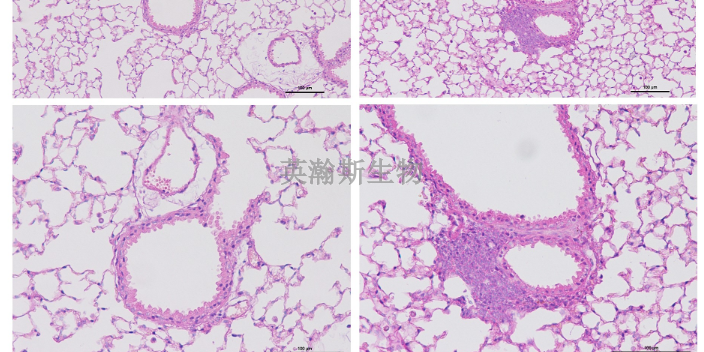
HE染色全名苏木精—伊红染色法,属于化学染色法,其主要依靠苏木精染液为碱性,主要使细胞核内的染色质与胞质内的核糖体着紫蓝色;伊红为酸性染料,主要使细胞质和细胞外基质中的成分着红色。实验过程:1、石蜡切片脱蜡至水:依次将切片放入二甲苯Ⅰ20min-二甲苯Ⅱ20min-无水乙醇Ⅰ5min-无水乙醇Ⅱ5min-75%酒精5min,自来水洗。2、苏木素染色:切片入苏木素染液染3-5min,自来水洗,分化液分化,自来水洗,返蓝液返蓝,流水冲洗。3、伊红染色:切片依次入85%、95%的梯度酒精脱水各5min,入伊红染液中染色5min。4、脱水封片:切片依次放入无水乙醇I5min-无水乙醇II5min-无水乙醇Ⅲ5min-二甲Ⅰ5min-二甲苯Ⅱ5min透明,中性树胶封片。5、显微镜镜检,图像采集分析。结果判读:细胞核呈蓝色,细胞质呈红色HE染色观察细胞形态变化。安徽值得信赖的HE染色公司
HE染色的实验目的以及实验结果分析。安徽值得信赖的HE染色公司
HE染色知识点1:对送检组织标本的要求送检组织标本在手术切除或活检后应当立即放入4%中性缓冲甲醛溶液中固定。尸检标本应当尽量在死亡后尽早取材固定。送检组织需要全部取材的,应当在送检单上注明,有特殊要求(如细菌培养、解释道化学分析等)应当事先联系,并且在标本未固定前进行处理。知识点2:组织取材要求在对送检组织标本进行详细检查的基础上,根据诊断的需要,确定取材的部位和块数。切取的组织应当按照不同的部位分别给予不同的编号或标记,以便镜检时核对。另外,尽可能在取材前对有意义的标本的表面及剖面镜下摄影,并编号存档南京英瀚斯,专业的病理染色实验服务平台。安徽值得信赖的HE染色公司