HE染色注意事项:1、染色时调节pH值很重要。如果组织块在福尔马林中固定时间长,组织酸化而影响细胞核着色。因此,要在自来水中冲洗时间长一些或在饱和碳酸锂水溶液中处理10-30min,这样可以使细胞核着色较深。染伊红时胞浆着色不佳,可在伊红溶液中滴加1-2滴冰醋酸。2、切片染苏木精后,分色这一步是关键,应在显微镜下控制进行,一般以细胞核染色清楚(晰)而细胞质基本无色为佳。如果过分延长分色时间将导致染色太浅,应重新染色后再行分色。3、切片经酒精脱水后,入二甲苯时可出现白色不透明状态,此为脱水不彻底,应将切片退回无水酒精,更换酒精、二甲苯,以求彻底脱水与透明。4、在染色过程中不要让切片干燥,以免切片收缩、变形,影响神经元形态。5、切片从二甲苯取出或进入二甲苯前,切片周边均应擦干净或吸干多余水分。6、***封固时,要用中性树脂,防止日后褪色,盖片要选大于组织块的面积,如漏出一部分不久将会褪色,所用树脂浓度要适当,树脂封固时不能有气泡。HE染色,优先南京英瀚斯生物。值得信赖的HE染色分析
HE染色常见问题:Q5:细胞核呈棕红色改变答:苏木素染液过度氧化;或苏木素染色后反蓝不足导致。应该立即更换苏木素染色液。或在流动自来水(一般自来水PH7.5-7.8),或在稀释的氨水溶液,或在0.2%碳酸氢钠中适当浸泡,这些步骤均可一定程度地加强苏木素染色后的反蓝效果。Q6:伊红染色较淡答:伊红的PH改变了(PH可能已大于5);或反蓝液体未漂洗干净,残留后影响胞浆嗜酸性染色;或者切片太薄并且在随后的脱水步骤停留过久。对策:检查伊红染色液PH,可采用乙酸调至4.6-5.0。根据以上提示,调整实验步骤。上海结果客观的HE染色价格HE染色规范化流程及注意事项?

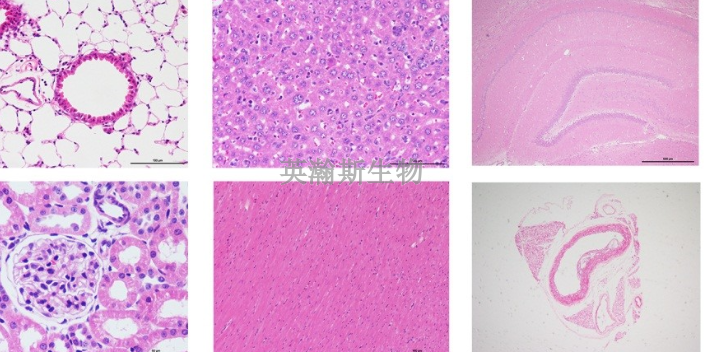
HE染色攻略:HE染色又称为苏木精-伊红染色,染色后组织或细胞可以借助普通光学显微镜观察与鉴别细胞凋亡与细胞坏死的一种染色方法。这种方法适用范围***,对组织细胞的各种成分都可着色,便于***观察组织构造,而且适用于各种固定液固定的材料,染色后不易褪色可长期保存。经过HE染色,细胞核被苏木素染成蓝紫色,细胞质被伊红染色呈粉红色。可以观察细胞结构、组织层次等等。首先切片组织是否完整,组织有无损伤;然后看切片有无刀痕;***细胞核是否清晰可见,胞核与包浆要对比鲜明。
HE染色观察细胞凋亡,凋亡检测中形态学方法是**直观、可靠的方法之一。对组织和各种细胞进行染色后,在光学显微镜、荧光显微镜或电子显微镜下观察,通过观察细胞的形态或染色的类型来判断凋亡的发生与否。细胞涂片或细胞甩片的制备:对于贴壁细胞,可将盖玻片放于培养器皿中,让培养细胞长于玻片上,然后用药物诱导细胞凋亡后取出,用4%多聚甲醛固定5min。对于悬浮细胞,用药物诱导细胞凋亡后,离心1000r/min收集细胞,用PBS洗2次,收集调整细胞数为1X105/ml,涂片或用离心甩片,用4%多聚甲醛固定5min;在光学显微镜下,贴壁细胞由原来的梭形或多角形变小、变圆,核呈蓝色或蓝黑色,胞浆呈淡红色,核固缩、破碎,形成凋亡小体等。悬浮细胞,整个细胞皱缩,核固缩,破碎,形成凋亡小体,染色质颜色加深等。常用HE染色试剂配制方法。
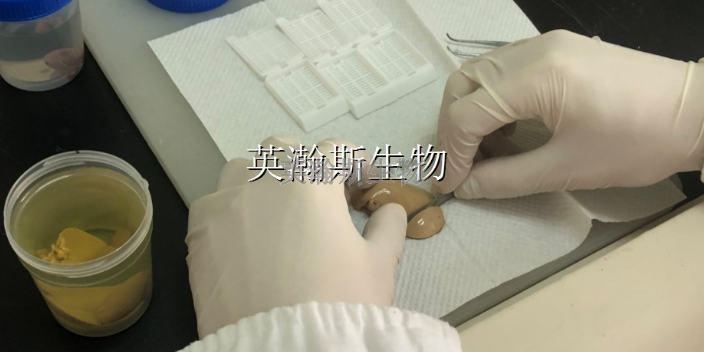
HE染色不管怎么操作,始终无法染色或淡染答:这种情况一般因为组织固定时采用了酸性甲醛;或者组织在甲醛中浸泡时间太长;或者久置的甲醛变性分解为甲酸。补救:防患于未然,要么使用新鲜的中性甲醛固定,要么在存放的甲醛中加一点碳酸钠中和甲酸。对于已经固定的组织可考虑再次固定;对于已经制出的片子,染色前采用5%重铬酸钾溶液浸泡半小时以上,然后自来水漂洗5min,可改善染色。也可以将切片放入3%硫酸铁铵溶液中,补充染色媒介,增强苏木素与组织的亲和力(苏木素染色必须要媒介才能染上,单纯的苏木素与组织的亲和力很弱)。让您放心的实验外包公司,专业HE染色实验服务平台。宁夏推荐的HE染色哪家好
心脏组织HE染色如何观察。值得信赖的HE染色分析
HE染色是目前国内外病理诊断上***采用的常规染色方法。切片质量的好坏,可直接影响疾病诊断的及时与准确性。因此,能制作出一张高质量的HE染色切片,是必须掌握的技术之一。送检样本经4%多聚甲醛固定,固定状态良好后,严格按照本单位病理实验检测SOP程序进行修剪、脱水、包埋、切片、染色、封片***镜检合格的样片。在显微镜下浏览切片或浏览数字切片,在不同倍数下详细观察组织切片情况,对切片中基本病理改变如充血、淤血、出血、水肿、变性、坏死、增生、纤维化、机化、肉芽组织、炎性变化等情况文字描述,并反映出片子之间的差异。对典型病变部位成像并在word文档中用箭头标识。值得信赖的HE染色分析