利用EAE动物模型,科学家们得以深入研究多发性硬化症(MS)对大脑认知功能的影响及其潜在干预手段。这一模型能够模拟MS患者大脑神经系统的病理变化,包括神经纤维的脱髓鞘、神经元损伤以及炎症反应等,从而为我们提供了一个独特的实验平台。通过观察EAE动物模型在认知任务中的表现,科学家们能够评估MS对大脑认知功能的损害程度,并探究其背后的神经生物学机制。同时,利用这一模型,科学家们还可以测试不同的干预手段,如药物疗愈、康复训练等,以评估它们对改善认知功能的效果。因此,利用EAE动物模型深入研究MS对大脑认知功能的影响及其潜在干预手段,对于推动MS的临床疗愈和研究具有重要意义。可以在猴、大鼠、小鼠等动物制备EAE模型。四川大鼠eae模型动物实验外包
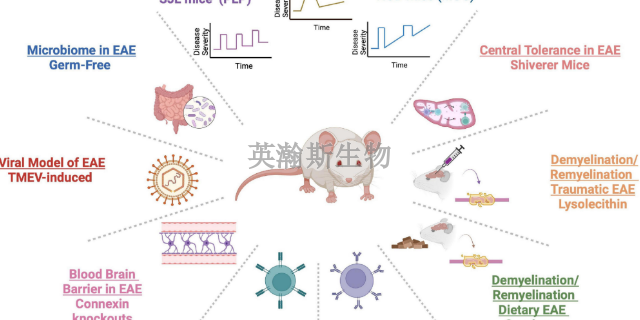
EAE动物模型,全称为实验性变形反应性脑脊髓炎动物模型,是神经科学研究领域中的一种重要工具。该模型通过模拟多发性硬化症(MS)等神经系统疾病的病理过程,为科学家们提供了一个独特的实验平台,使他们能够深入研究这些疾病的发病机制、病理变化以及疗愈策略。EAE动物模型不仅可以帮助科学家们揭示MS等疾病的发病机理,还可以为开发新的疗愈方法和药物提供重要线索。通过调控模型动物的免疫反应、观察神经系统的再生和修复过程,科学家们可以评估不同疗愈方法的疗效,为MS患者的疗愈提供更为精细和个性化的方案。因此,EAE动物模型在神经科学研究领域具有广泛的应用前景和深远的意义。四川大鼠eae模型动物实验外包EAE模型是人类MS的经典动物模型,能够为MS提供充分的实验依据。
EAE模型的发展与年龄密切相关。幼龄动物发病后症状很快达到高峰,随后又迅速恢复,和成年动物相比病程较短,其抗原注射部位及CNS内的炎性细胞浸润程度较轻,并且幼龄动物体重偏小,一般情况差,易出现麻醉意外而死亡。若动物体重(周龄)偏大,则发病延迟,且症状较重,所以选择受试动物以青年期为佳。但若作为抗原提供者,其年龄可适当放宽,一般大于4周即可。MS多为青年女性,EAE的发生也存在性别差异。一般来讲,雌性动物较雄性敏感,表现在雌性动物的发病率高,临床症状相对严重,如Wistar大鼠及SJL/J小鼠,但也有的动物如Lewis大鼠,雄性较雌性敏感。另外实验时间选择在夏季比冬春季节诱导动物模型的敏感性更高。敏感性高的动物,有时症状较严重且死亡率高,应引起注意。
常用的致敏抗原有髓鞘碱性蛋白(MBP)或其多肽片断(如MBP peptide 89—101)以及蛋白脂(PLP)等。长期以来MBP和PLP被认为是引起EAE和MS的主要抗原,MBP是髓鞘中抗原性比较强的蛋白质,占髓鞘总蛋白的40%,等电点在10以上,是强碱性蛋白质。研究表明MBP可***体内Th+细胞,使之穿过血脑屏障,攻击自身神经髓鞘的MBP,从而导致***白质脱髓鞘,引起EAE模型或MS。近年来多用MBP肽代替MBP免疫动物。PLP是高度疏水的膜蛋白,对PLP不同肽决定簇发生反应的CD4+T细胞能诱导急性、慢性复发型及慢性进展型EAE。在MS患者体内也发现与PLP抗原决定簇发生反应的T细胞。 用大鼠制备EAE模型有许多优点,如品系多,选择余地大,繁殖快,同一品系中个体间差异小,实验方便。
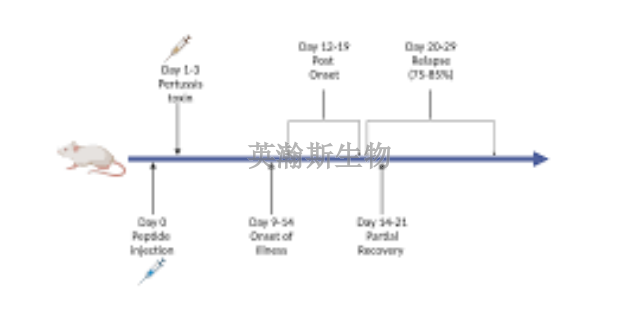
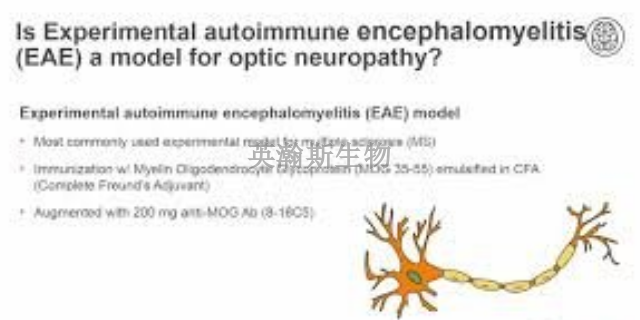
通过对EAE动物模型的深入研究,科学家们有望为多发性硬化症(MS)患者带来更加有效的疗愈方法和更好的生活质量。EAE动物模型作为模拟MS病理过程的重要工具,为科学家们提供了一个独特的实验平台,使他们能够更深入地了解MS的发病机制和疗愈靶点。通过深入研究EAE动物模型的病理变化、免疫反应以及神经再生等方面,科学家们可以筛选出潜在的疗愈药物或方法,并评估其疗效和安全性。这些研究成果有望为MS患者提供更加个性化和精细的疗愈方案,帮助他们减轻症状、延缓病情进展,并提高他们的生活质量。因此,对EAE动物模型的深入研究将为MS患者带来希望,并为未来的医学进步开辟新的道路。用髓鞘少突胶质细胞糖蛋白35-55(MOG35-55) 多肽免疫C57BL/6小鼠建立实验性自身免疫性脑脊髓炎EAE模型。重庆eae模型造模方法
EAE模型是常用的实验性动物模型用来研究人炎症脱髓鞘。四川大鼠eae模型动物实验外包
目前主要由三种髓鞘蛋白(或蛋白多肽)用于诱发EAE模型的研究:髓鞘少突胶质细胞糖蛋白(MOG),髓鞘碱性蛋白(MBP)和髓鞘蛋白脂质蛋白(PLP)※MBP是**早用来EAE研究的髓鞘抗原,多以诱发急性EAE(AcuteEAE)模型。※MOG是目前常用建立EAE模型的髓鞘抗原,多以诱发慢性EAE(ChronicEAE)模型※PLP也是常用建立EAE模型的髓鞘抗原,模型呈现缓解-复发的特点,多用来建立复发-缓解型(RelapseremittingEAERR-EAE)模型。以上三种是常见的诱导eae模型的蛋白。四川大鼠eae模型动物实验外包