EAE动物模型的研究不仅对于多发性硬化症(MS)的疗愈具有重要的推动作用,更可能为其他神经系统疾病的研究提供宝贵的启示。通过对EAE动物模型的深入研究,科学家们能够更深入地理解神经系统疾病的发病机制,从而为开发新的疗愈策略提供理论支持。同时,EAE动物模型在模拟神经系统疾病病理过程方面的成功应用,也为其他类似疾病的研究提供了可借鉴的经验和方法。通过借鉴EAE动物模型的研究思路和技术手段,科学家们可以更加高效地开展其他神经系统疾病的研究,为这些疾病的诊断和疗愈提供新的思路和方向。因此,EAE动物模型的研究不仅局限于MS的疗愈,更有着广泛的应用前景和深远的意义。eae模型还可以研究炎症和髓鞘再生的解决反调节机制。重庆推荐的eae模型有哪些

比较不同的神经功能损伤评分标准对小鼠实验性自身免疫性脑脊髓炎(EAE)运动功能障碍评估的效能。方法:应用MOG35-55多肽加完全福氏佐剂乳化后免疫20只C57BL/6小鼠,复制EAE小鼠模型,并使用3种不同的评分标准(Kono's5分法、Hooper's7分法、Weaver's15分法)观察和评估实验动物的发病情况,对实验小鼠在发病初期、高峰期的神经功能障碍进行定量的功能损伤评价。结果:3种评分标准比较,在发病初期,15分法和7分法评估神经损伤症状的敏感性相当,比5分法高;高峰期,以症状评分与病理评分的相关性程度来比较3种评分法的效度,15分法效度比较高,7分法次之。结论:Weaver's15分法评价EAE模型神经功能损伤症状,具有明显的优势,推荐作为今后EAE研究的优先评分法。重庆推荐的eae模型有哪些通常采用主动诱导法制备EAE模型,将抗原与佐剂的混合乳剂直接注射至动物体内。
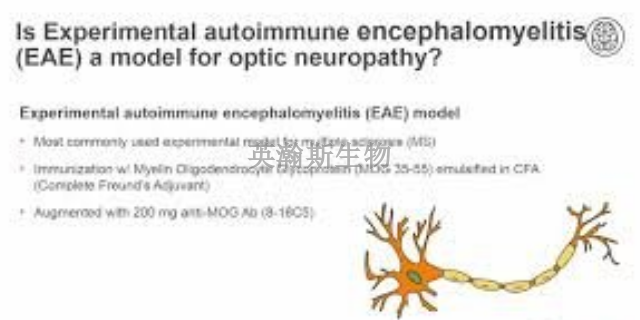
实验性***反应性脑脊髓炎(EAE)是一种以特异性致敏的CD4+T细胞介导为主的,以***系统内小血管周围出现单个核细胞浸润及髓鞘脱失为特征的自身免疫性疾病,是人类多发性硬化(MS)的理想动物模型,在临床神经免疫学的研究中具有重要意义。实验性***反应性脑脊髓炎(EAE)是一种以特异性致敏的CD4+T细胞介导为主的,以***系统内小血管周围出现单个核细胞浸润及髓鞘脱失为特征的自身免疫性疾病,是人类多发性硬化(MS)的理想动物模型,在临床神经免疫学的研究中具有重要意义。
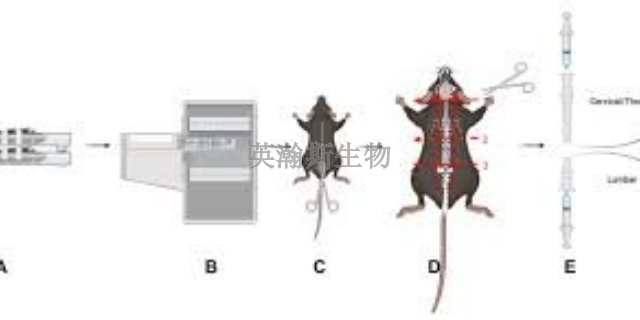
EAE模型是实验动物通过神经组织(其中的某些成分)或病毒诱导产生的。EAE的诱导有主动诱导法和被动诱导法两种。不同的免疫方法,可影响抗原递呈,激发不同的免疫反应,这不但影响EAE的发生率,还可影响其发展与转归。通常采用主动诱导法制备EAE模型,将抗原与佐剂的混合乳剂直接注射至动物体内,经过一定时间的潜伏期,诱导EAE的产生。抗原注射部位的不同,可影响EAE的发生率、潜伏期、死亡率及复发率。常用的注射部位有脚垫、颈部及背部(皮下、皮内、肌肉)、腹腔和尾静脉等多种,其中以皮下多点注射及脚垫注射的发病率比较高,而颈部注射则有较高的复发率。 因多次注射易引发免疫耐受,现在多采用单次注射抗原法。胶原纤维酸蛋白(GFAP)也参与EAE模型的诱发。
从鸟类到哺乳类的多种动物如鸡、小鼠、大鼠、豚鼠、家兔、羊、犬、猴等均可成功诱发EAE,但不同种属或同一种属不同品系动物的敏感性有很大差异。对EAE敏感的动物有Lewis、DA大鼠,PL/J、SJL/J小鼠,Hartley、Strain13豚鼠。虽然豚鼠对诱发EAE相当敏感,但其品系复杂,有关试剂缺乏,一般不常用作实验对象。相比之下大鼠及小鼠的背景知识及相关试剂则较为普遍,遗传学、免疫学等方面的研究也较深入,且其EAE在临床、病理、免疫及生化改变等方面都与人类脱髓鞘疾病较为相似,因此应用比较为普遍。用髓鞘少突胶质细胞糖蛋白35-55(MOG35-55) 多肽免疫C57BL/6小鼠建立实验性自身免疫性脑脊髓炎EAE模型。重庆推荐的eae模型有哪些
小鼠、大鼠、豚鼠、家兔、羊、犬、猴等均可成功诱发EAE,在选择动物时需要寻找EAE模型的敏感动物。重庆推荐的eae模型有哪些
科学家们可以通过精心调控EAE动物模型的免疫反应,深入研究免疫疗法在多发性硬化症(MS)疗愈中的潜在应用。在EAE动物模型中,科学家们能够模拟MS患者体内免疫系统的异常反应,并通过一系列实验手段,精细地调控免疫细胞的活性、数量和功能。通过观察调控免疫反应后EAE动物模型的病情变化,科学家们能够评估不同免疫疗法对MS的疗愈效果,并探索其背后的作用机制。这一研究不仅有助于揭示MS的发病机制,还为开发新的免疫疗法提供了重要的实验依据。因此,通过调控EAE动物模型的免疫反应来研究免疫疗法在MS疗愈中的应用,对于推动MS的疗愈进展具有重要意义。重庆推荐的eae模型有哪些