- 产地
- 苏州
- 品牌
- 外泌体提取试剂
- 型号
- 齐全
- 是否定制
- 是
外泌体的提取方法:1、磁珠免疫法。外泌体表面有其特异性标记物(如CD63、CD9蛋白),用包被抗标记物抗体的磁珠与外泌体囊泡孵育后结合,即可将外泌体吸附并分离出来。磁珠法具有特异性高、操作简便、不影响外泌体形态完整等优点,但是效率低,外泌体生物活性易受pH和盐浓度影响,不利于下游实验,难以普遍普及。2、多聚物沉淀法。聚乙二醇(PEG)为常用的多聚物,可与疏水性蛋白和脂质分子结合共沉淀,早先应用于从血清等样本中收集病毒,现在也被用来沉淀外泌体,其原理可能与竞争性结合游离水分子有关。利用PEG沉淀外泌体存在不少问题:比如纯度和回收率低,杂蛋白较多(假阳性),颗粒大小不均一,产生难以去除的聚合物,机械力或者吐温-20等化学添加物将会破坏外泌体等。外泌体提取:聚乙二醇(PEG)为常用的多聚物,可与疏水性蛋白和脂质分子结合共沉淀。广州正规外泌体提取试剂厂家供应

外泌体的提取、分离方法:聚合物沉淀法。聚合物沉淀法用于分离病毒和其他的生物大分子已有50多年历史,近几年,将其作为一种新的方法来分离外泌体。目前,市场已经有应用聚乙二醇(polyethyleneglycol,PEG)溶液提取外泌体的试剂盒,较常见的是SystemBiosciences公司的ExoQuick®和ExoQuick-TC®kits,该试剂盒操作简单不需要特殊的仪器,但是价格昂贵。提取外泌体的试剂盒主要成分是PEG8000(30%~50%),将试剂盒与体液或细胞培养液4℃孵育过夜,之后再低速离心。上海正规外泌体提取试剂价格外泌体提取:免疫分离外泌体的原理大多是通过抗体包被的微球,特异性结合外泌体。

外泌体与免疫系统:不同的细胞来源的外泌体,包括免疫细胞(B细胞和树突状细胞)、病细胞、上皮细胞和间充质细胞,释放出带有载体的外泌体,可影响先天免疫系统和适应性免疫系统中受体细胞的增殖和各自的活性。CD4+和CD8+T细胞可直接或间接地受到外泌体的影响,刺激或压制其增殖和功能。外泌体与代谢性和心血管疾病:外泌体可以通过携带miRNA或代谢物分子在代谢性疾病和心血管疾病的发生的发展过程中起作用。体外培养心血管疾病的细胞收集的外泌体与疾病相关的代谢适应有关;体外培养的间充质干细胞和胚胎干细胞的外泌体具有保护心血管的作用。这些发现表明不同来源的外泌体可以通过传递miRNA,蛋白等物质改变受体细胞的代谢状态。外泌体检测作为一种新型的液体活检热点技术已被许多临床科研机构普遍地应用于一些病症和疾病的无创诊断。
外泌体的提取分离:1、超滤离心。由于外泌体是一个大小约几十纳米的囊状小体,大于一般蛋白质,利用不同截留相对分子质量(MWCO)的超滤膜对样品进行选择性分离,便可获得外泌体。超滤离心法简单高效,且不影响外泌体的生物活性,是提取细胞外泌体的一种新方法。2、磁珠免疫法。外泌体表面有其特异性标记物(如CD63、CD9蛋白),用包被抗标记物抗体的磁珠与外泌体囊泡孵育后结合,即可将外泌体吸附并分离出来。磁珠法具有特异性高、操作简便、不影响外泌体形态完整等优点,但是效率低,外泌体生物活性易受pH和盐浓度影响,不利于下游实验,难以普遍普及。目前人们多采用超速离心、免疫磁珠、超滤、沉淀或试剂盒等方法实现外泌体的提取分离。

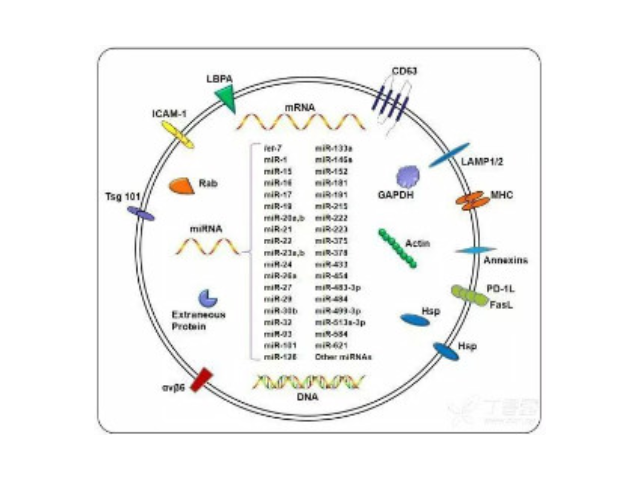
首先在无菌条件下提取人体体液,并用PBS缓冲液进行稀释,然后通过离心筛选初步去除体液中的细胞成分和细胞碎片,制成体液样本备用;体液样本纯化:通过过滤膜对上述体液样本进行过滤,进一步去除体液中的细胞残片及其他杂质,静置10~15分钟,留取沉淀物备用;外泌体提取:将上述沉淀物用PBS缓冲液进行悬浮,使外泌体悬浮于液体上层,然后用无菌针管吸取上层含有外泌体的液体,置于80℃储存备用。此提取方法条件复杂,成本高,专利申请利用静置不太可能把外泌体沉降下来;根据外泌体表面的特异生物化学特性通过提取试剂的特异配方把外泌体从水相中沉降下来。活细胞分泌到胞外的囊泡样小体,含有多种蛋白和核酸分子(DNA、RNA、以及miRNA)。北京外泌体提取试剂单价
形成了一种全新的细胞间信息传递系统,影响细胞的生理状态并与多种疾病的发生与进程密切相关。广州正规外泌体提取试剂厂家供应
外泌体的提取、分离方法:微流控技术。微流控是利用微纳米级尺寸的管道来处理和操控流体所涉及的一门技术,其在外泌体分离方面的应用受到越来越多学者的关注。Jie等[16]课题组开发了一种三维纳米结构微流控芯片,微柱阵列通过化学沉积将交叉多壁碳纳米管功能化,然后其就可以识别特定的分子(CD63)并利用独特拓扑纳米材料高效的捕获外泌体。Wunsch等[17]利用硅工艺生产纳米级确定性侧向位移(Nano-DLD)芯片,得到了均匀的间隙尺寸,该芯片可以灵敏地将20~110nm的颗粒分离。该研究证明了外泌体基于大小的位移,从而揭示了利用芯片分选和量化纳米级生物胶体的潜力。广州正规外泌体提取试剂厂家供应
密度梯度离心法该方法由于比较繁琐,用的较少。原理是:像所有的脂质小囊泡一样,外泌体可以悬浮于特定密度梯度的蔗糖中,其密度范围1.13g/ml-1.21g/ml,将要分离外泌体的样本液体置于梯度蔗糖介质上,随后通过离心将外泌体分离。此法获得的外泌体纯度较高,但步骤繁琐,耗时,对离心时间极为敏感。具体步骤是:收集培养2d的上清液。将培养上清液先以1500r/min离心5min除去细胞及碎片,再依次以1000×g离心10min取上清,10000×g离心30min取上清,然后用100ku超滤离心管(Millipore)浓缩至15mL,主要来源于细胞内内溶酶体微粒内陷形成的多囊泡体,经多囊泡体外膜与细胞...
- 太原外泌体提取试剂厂家推荐 2026-05-02
- 南京正规外泌体提取试剂哪里买 2026-05-01
- 贵阳外泌体提取试剂厂家批发价 2026-05-01
- 长沙正规外泌体提取试剂哪家便宜 2026-05-01
- 珠海外泌体提取试剂直销厂家 2026-04-30
- 成都正规外泌体提取试剂厂家批发价 2026-04-30
- 南京外泌体提取试剂生产厂家 2026-04-29
- 武汉外泌体提取试剂厂家供应 2026-04-29
- 广州外泌体提取试剂哪里买 2026-04-29
- 宁波外泌体提取试剂供应商 2026-04-29
- 厦门正规外泌体提取试剂厂家推荐 2026-04-28
- 郑州正规外泌体提取试剂报价 2026-04-28
- 郑州正规外泌体提取试剂哪家好 2026-04-28
- 金华外泌体提取试剂进货价 2026-04-28
- 杭州正规外泌体提取试剂直销厂家 2026-04-28
- 徐州外泌体提取试剂进货价 2026-04-27


- 杭州细胞高效转染试剂哪里买 05-03
- 青岛细胞外基质胶供应商 05-03
- 长沙细胞外基质胶直销价 05-03
- 重庆正规鼠尾胶原产品介绍 05-03
- 广州原代细胞分离试剂盒厂家推荐 05-02
- 芜湖太原原代细胞分离试剂盒 05-02
- 重庆正规原代细胞分离试剂盒厂家 05-02
- 太原外泌体提取试剂厂家推荐 05-02
- 宁波长沙原代细胞分离试剂盒 05-02
- 唐山原代细胞分离试剂盒进货价 05-02