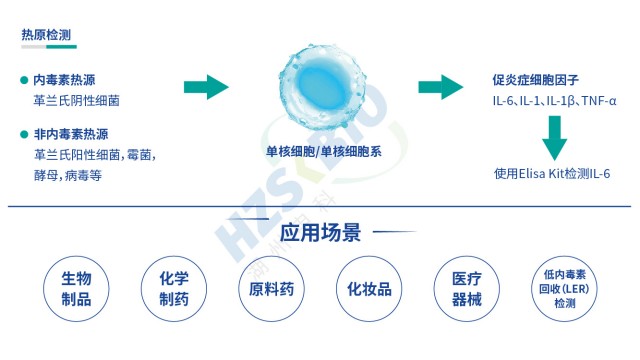
热原是指微量即可引发恒温动物体温异常升高的物质,分为内源性(如细胞因子)与外源性两类,外源性热原又涵盖微生物来源(革兰氏阴性菌脂多糖 LPS、革兰氏阳性菌脂磷壁酸 LTA、病毒、真菌等)与非微生物来源(灰尘、橡胶降解产物等)。传统细菌内毒素检查法(BET)只能检测革兰氏阴性菌的 LPS,无法覆盖非内毒素热原,而单核细胞活化试验(MAT)可弥补这一缺陷。其原理是:热原通过活化单核细胞表面的 Toll 样受体(TLR,如 TLR4 识别 LPS、TLR2/TLR6 识别 LTA),启动先天免疫反应,促使细胞释放 IL-6、TNF-α 等促炎细胞因子;随后采用 ELISA 法检测 IL-6 浓度,结合 LPS 标准曲线推算样品中总热原含量,实现对内毒素与非内毒素热原的同步检测,契合《中国药典》9301 指导原则中 全场景防控热原风险”的要求。
2023年PRIMM研究:聚山梨酯80 mRNA疫苗中,家兔法热原检查因LER漏检41%,MAT回收率98%+。非动物源热原检测操作步骤
家兔热原试验作为热原检测领域的 “法定传统方法”,被中国药典(ChP)、美国药典(USP)、欧洲药典(EP)均列为法定检测项目,其主要优势在于可通过家兔体温应答筛查所有类型热原,尤其适用于无法排除非内毒素热原污染的高风险产品,如血液制品、放射性质药物及部分生物制剂。然而,家兔热原试验存在明显局限:动物个体差异大,需额外投入时间与成本筛选合格家兔;检测周期长(至少 6 小时),无法满足生物制品快速放行需求;灵敏度较低(对 LPS 检测限≥5EU/kg),与全球倡导的“动物福利3R原则”背道而驰。
江苏原料药热原检测结果判定热原检测历经动物整体试验、体外生化反应到细胞免疫应答的三阶段演进,灵敏度与效率不断提升。
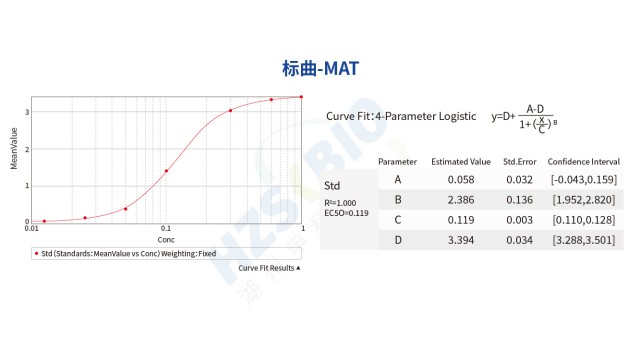
MAT法热原检测特定标准品与传统细菌内毒素国家标准品存在本质差异,需明确区分以保障检测准确性。MAT 特定标准品为大肠杆菌(E.coli 0113:H10:K)菌株制备,经全国 5 家药品检验所(含中检院)用凝胶法、动态浊度法及动态显色法协作标定,溯源至国际标准品,可同时检测内毒素与非内毒素热原;而传统细菌内毒素国家标准品(如 9000EU 规格)源自大肠杆菌(E.coli O111:B4),只适用于内毒素检测,无法识别非内毒素热原。关键验证数据显示,用 MAT法检测 9000EU 内毒素标准品时,加标回收率不在 50%-200% 的合格范围,因此不能替代 MAT 特定标准品。值得注意的是,尽管 MAT 试剂盒用内毒素标准品绘制标曲,但经验证其可识别非内毒素热原—若样品中存在非内毒素热原(如革兰氏阳性菌的脂磷壁酸),会触发细胞阳性反应,有效避免漏检,这也是 MAT 法在热原防控中优于单一内毒素检测的关键优势。
MAT法热原检测中,标曲信号值偏低或线性不佳是常见问题,需按细胞、标准品、ELISA 检测三环节排查解决。细胞相关问题中,细胞复苏后若未充分混匀导致结团,种板后细胞分布不均,会使局部信号弱,需振荡细胞悬液后再种板;细胞活性差或处理时间超半小时,会降低炎症因子分泌,需严格按说明书操作并缩短处理时间;孵育未达 37℃、5% CO₂条件,细胞活化不足,需确保培养箱参数稳定;细胞悬液若接触外源热原,会引发非特异性反应,操作时需远离热原污染源。标准品问题方面,配制稀释错误会直接导致浓度不准,需核对稀释步骤;振荡时间不足(未按说明书要求)会使内毒素分散不均,需确保振荡充分且 4 小时内使用;标准品降解会导致效价下降,需按推荐条件保存(如 - 20℃冷冻)。ELISA 检测环节,孵育时间短或振荡速度慢会影响抗体结合,可适当延长孵育或提高振荡速度;TMB 显色不足(<3 分钟)会导致信号低,需显色 3-10 分钟,待高浓度点 OD600 达 1.0 时加终止液。
热原有广谱来源特征,革兰阴性菌(内毒素/LPS)致热能力强,革兰阳性菌、真菌、病毒均可产生。
PBMC(外周血单个核细胞)用于 MAT 热原检测时,存在异质性与血源供应两大关键问题。从异质性来看,PBMC 含 12% 单核细胞与 88% 淋巴细胞,且来自不同供体,细胞组成、功能状态及热原反应存在明显差异,导致热原刺激后 IL-6 释放量波动大,标准化难度高。血源供应方面,除受献血者数量、时间及采集血液政策限制外,EP2.6.30 还要求严格检测乙肝、丙肝等标志物,且采集血液、处理、试剂制备全程需无菌操作,流程环节多、复杂度高,远不及单核细胞系制备简便,易影响热原检测的时效性与稳定性。欧洲药典已正式废除家兔法热原检测,推荐单核细胞活化反应试验(MAT)为合适的替代方案。江苏原料药热原检测风险评估
鲎试验法(LAL)法进行热原检测灵敏度高、操作方便,但只针对内毒素,易受干扰且有 LER 现象。非动物源热原检测操作步骤
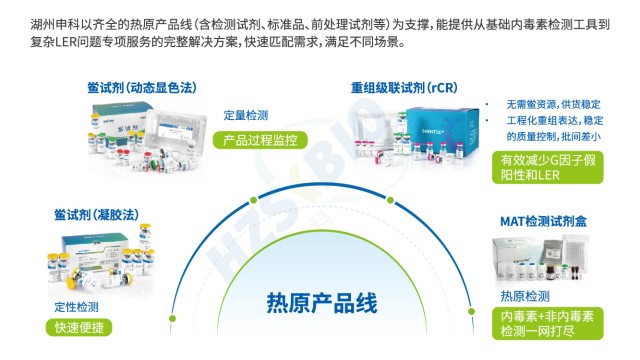
传统细菌内毒素检查法(BET)只能检测革兰氏阴性菌的 LPS,无法识别革兰氏阳性菌 LTA、真菌酵母多糖、病毒鞭毛蛋白等非内毒素热原,存在漏检风险;同时,部分样品(如脂质体、表面活性剂制剂)会因内毒素吸附导致低内毒素回收(LER),BET法难以准确定量。MAT 法通过单核细胞表面的多种 TLR 受体(TLR1-TLR10),可识别不同类型热原:TLR4 识别 LPS、TLR2/TLR6 识别 LTA 与酵母多糖、TLR5 识别鞭毛蛋白、TLR3 识别病毒 dsRNA 等,实现 “全热原覆盖”。湖州申科生物热原检测试剂盒(MAT法)的验证数据显示,其对不同浓度非内毒素热原均有响应:如 0.1-100μg/mL 鞭毛蛋白可检测到 0.005-0.035EU/mL热原活性,0.1-10μg/mL LTA 对应 0.1-0.7EU/mL 热原活性,1-100μg/mL 雷西莫特(TLR7/8 配体)对应 0.5-3.0EU/mL 热原活性。此外,MAT法检测的是热原的生物活性(而非单纯 LPS 含量),可避免 LER 导致的假阴性,为CGT等高风险产品提供更有保障的热原检测方案。
非动物源热原检测操作步骤