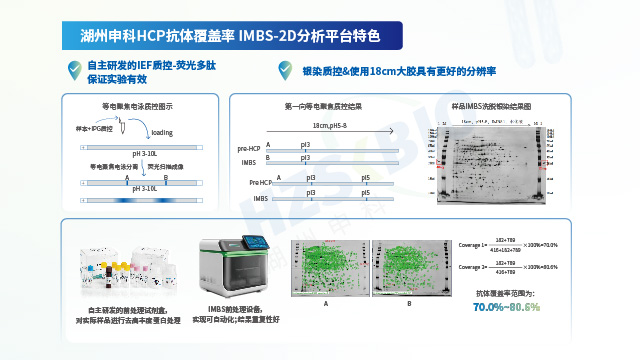
湖州申科生物结合不同宿主实际的生产工艺,通过高质量免疫原和 HCP 多抗的标准化制备流程,获得高效价、高覆盖率的抗体,开发了适用于大肠杆菌表达菌 (BL21) 生产工艺、克隆菌碱裂法提取质粒工艺的 SHENTEK®E.coli HCP检测试剂盒, 适用于CHO\MDCK\HEK293\Sf9\VERO\毕赤酵母等不同宿主的 HCP 检测试剂盒。用于中间品、原液及终产品等的HCP定量监测。为确保 ELISA 对HCP定量检测的准确性,须对 HCP 抗体覆盖率进行验证。湖州申科抗体覆盖率平台采用2D Clean-up 试剂盒去除蛋白样品的干扰物(洗涤剂、盐、脂质、酚类和核酸等离子污染物),并设置2D 质控标准品进行严格质控,同时以阴性抗体为对照平行试验,以提高结果准确度。
HCP具有异质性,体现在分子本身的多样性以及和工艺相关的变异性。成都工艺特异型宿主细胞蛋白(HCP)残留检测免疫策略
为了更好地控制工艺和保证产品质量的稳定,各国监管机构均要求提供使用的宿主细胞蛋白残留检测ELISA试剂盒的抗体覆盖率数据。一般需进行覆盖率分析的场景一般有以下几种情况:①临床II期后,若是继续使用商品化试剂盒,则需要评估试剂盒抗体覆盖率是否可以继续用于质量监控;②临床III期及以后阶段,产品研究者开发了平台化或工艺专属型的HCP监测方法,该类试剂盒在使用前要评估覆盖率水平与商业化覆盖水平的差异;③申报时没有提交覆盖率数据,监管机构可能会对企业提出发补的要求;④产品上市后发生了包括生产场地变更,工艺变更,HCP分析方法变更等因素的变更,研究者则需要评估变更前后抗体覆盖率水平的差异,以及该差异对药品质量与安全带来的影响。
上海Hi-5宿主细胞蛋白(HCP)残留检测常见问题分析HCP检测的经典方法是ELISA法,但该方法在检测过程中存在漏检风险,需要对试剂盒抗体进行抗体覆盖率评估。
按照美国药典1132章节的要求,HCPs校准品需满足代表性要求,即能覆盖实际工艺产品生产中的HCPs。从HCP免疫检测方法使用目的和预期风险管理要求考虑,满足工艺开发和验证,同时为了应对下游工艺中潜在的异常工艺失效,或工艺变更需求,建议采用上游发酵工艺末端,如澄清处理后工艺点的样本作为HCPs的来源。在实际制备中,可采用空细胞或空载细胞在模拟实际工艺的预定条件进行采集,通过二维电泳或高分辨率质谱等蛋白质组学方法进行模拟工艺和实际工艺下HCPs的代表性表征分析。越靠近下游HCPs蛋白种类越少,也越接近DS中HCPs,但是其可能无法满足工艺开发和验证需求,也无法保证工艺的潜在风险,往往不推荐使用,或只作为上游工艺HCPs免疫检测法的辅助使用。
湖州申科生物CHO-K1 HCP 残留检测试剂盒(一步酶联免疫吸附法)基于固相酶联免疫吸附分析法,适用于基于CHO-K1细胞生产的生物制品中宿主残留蛋白的定量检测。该分析方法通过在预包被抗CHO-K1HCPs绵羊多抗的酶标板中加入校准品或待测样品、HRP标记的抗CHO-K1HCPs绵羊多抗进行共孵育。洗涤后,加入TMB底物进行显色反应,再使用终止液终止酶催化反应。利用酶标仪在450nm波长下测读吸光度,其吸光度与校准品或待测样品中的HCPs浓度成正相关,通过校准品拟合的剂量-反应曲线即可计算得出待测样品中HCPs的浓度。本试剂盒对待测样品无需进行特殊处理,只需通过合适的稀释比例进行适用性验证即可直接使用。本试剂盒操作步骤少,快速,检测专一性强,性能稳定可靠。
湖州申科HCP试剂盒开发经抗原表征、抗体制备到体系验证,全流程符合法规要求。
宿主细胞蛋白(HCPs)是生物制品生产过程中产生的关键工艺相关杂质之一,可导致患者不良的免疫反应、超敏反应,另外也存在导致产品蛋白的降解等问题,影响产品的安全性和有效性,是一项关键质控指标。HCPs残留检测应用常用的方法是ELISA法,操作简单、灵敏度高,通量较高,是HCPs残留检测的日常放行检方法,各国药典规定了用酶联免疫法进行HCPs残留检测。然而,ELISA 方法检测HCP残留仍面临诸多挑战。在实际的工艺生产过程中,宿主来源、生产工艺、纯化方式、生产规模等因素均可能对HCPs的种类及复杂性产生影响。
HCP 定制化开发需构建成熟平台、技术实力、合规体系、稳定供应、专业团队及成功案例的全维度支撑体系。单抗药物用宿主细胞蛋白(HCP)残留检测桥接验证
湖州申科自主研发IMBS抗体覆盖率检测法及低丰度HCP富集技术,合作完成多项课题并发表成果。成都工艺特异型宿主细胞蛋白(HCP)残留检测免疫策略
在宿主细胞蛋白(HCP)残留检测的分析方法中, ELISA方法是广泛应用的,并作为QC日常放行检测的主要手段。ELISA方法相对简单、精度良好,方便设定控制范围和建立技术规范,适用于产品开发和过程控制;但ELISA方法检测依靠抗原抗体特异性结合,因此用存在于生物制品中的HCPs作为免疫原生产出的抗体质量至关重要。无论是商品化ELISA试剂盒,还是自制的多克隆抗体,如果抗体的特异性和适用性不够高,都有可能带来HCPs漏检的风险,从而对生物制品质量安全带来风险。除此之外,ELISA检测HCPs使用多克隆抗体,无法针对性的提供高风险HCPs残留蛋白真实存在情况。
成都工艺特异型宿主细胞蛋白(HCP)残留检测免疫策略