大肠埃希氏菌(Escherichia coli,E. coli )又称大肠杆菌,其作为模式微生物被广泛应用于生命科学研究中。大肠杆菌是表达药用异源蛋白的常用微生物,在被批准的药用蛋白中,大约30%的产品以大肠杆菌作为表达宿主菌。与其他表达平台一样,尽管下游复杂的纯化步骤已经去除了大量的杂质,但终产品中仍会存在HCP残留风险,必须对其进行质量控制,使其符合放行标准。湖州申科生物E.coli表达菌HCP残留检测试剂盒用于大肠杆菌表达菌株BL21来源的宿主细胞蛋白定量检测,适用于重组蛋白类产品的工艺中间品和原液类样品,如白细胞介素(IL)、干扰素(rhIFN)、粒细胞-巨噬细胞集落刺激因子(rhGM-CSF)、肿瘤坏死因子(rhTNF)、促生长因子(EGF/FGF/PDGF)等。试剂盒检测步骤少,快速,专一性强,性能稳定可靠。
湖州申科拥有自主搭建的多克隆抗体库(CHO\E.coli\293T细胞等),提供对应覆盖率验证服务。江苏宿主细胞蛋白(HCP)残留检测方法对比
宿主细胞蛋白(HCPs)是生物制品生产过程中产生的关键工艺相关杂质之一,可导致患者不良的免疫反应、超敏反应,另外也存在导致产品蛋白的降解等问题,影响产品的安全性和有效性,是一项关键质控指标。HCPs残留检测应用常用的方法是ELISA法,操作简单、灵敏度高,通量较高,是HCPs残留检测的日常放行检方法,各国药典规定了用酶联免疫法进行HCPs残留检测。然而,ELISA 方法检测HCP残留仍面临诸多挑战。在实际的工艺生产过程中,宿主来源、生产工艺、纯化方式、生产规模等因素均可能对HCPs的种类及复杂性产生影响。
广东工艺特异型宿主细胞蛋白(HCP)残留检测试剂盒开发要求遵循严格且科学的宿主细胞蛋白残留检测标准,是确保产品顺利达标的重要基础条件。
毕赤酵母(Pichia pastoris)是第二代酵母表达系统中的代表性菌株,是美国FDA认定的GRAS(Generally Recognized As Safe)微生物,具有表达水平高,产物活性好,培养成本低,易扩大为工业化生产等特点。在生物制药领域,酶制剂、胰岛素、表皮生长因子、胶原蛋白等多种生物制剂已经通过毕赤酵母系统进行商业化生产。与其他产品杂质一样,毕赤酵母宿主残留蛋白(HCP)可能对生物制品的安全性和有效性产生不利影响,因此在生产监测、产品放行等过程中需要对其进行定量研究并进行严格控制。SHENTEK®毕赤酵母HCP残留检测试剂盒(一步酶联免疫吸附法)是湖州申科生物自主研发、具有完全自主知识产权的、实现关键试剂全国产化的毕赤酵母HCP通用检测试剂盒。本试剂盒适用于基于GS115、X33等在内的毕赤酵母菌株生产的生物制品中宿主残留蛋白的定量检测,操作步骤少、快速,检测专一性强,性能稳定可靠。
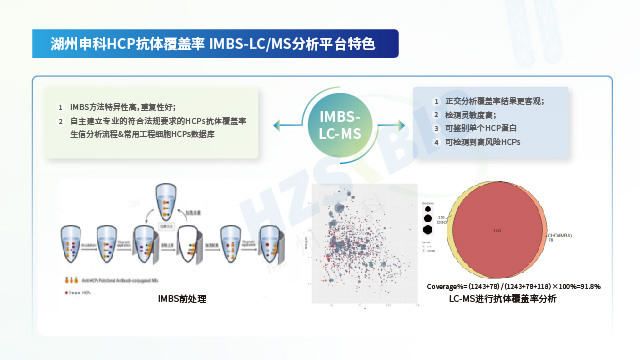
湖州申科生物结合不同宿主实际的生产工艺,通过高质量免疫原和 HCP 多抗的标准化制备流程,获得高效价、高覆盖率的抗体,开发了适用于大肠杆菌表达菌 (BL21) 生产工艺、克隆菌碱裂法提取质粒工艺的 SHENTEK®E.coli HCP检测试剂盒, 适用于CHO\MDCK\HEK293\Sf9\VERO\毕赤酵母等不同宿主的 HCP 检测试剂盒。用于中间品、原液及终产品等的HCP定量监测。为确保 ELISA 对HCP定量检测的准确性,须对 HCP 抗体覆盖率进行验证。湖州申科抗体覆盖率平台采用2D Clean-up 试剂盒去除蛋白样品的干扰物(洗涤剂、盐、脂质、酚类和核酸等离子污染物),并设置2D 质控标准品进行严格质控,同时以阴性抗体为对照平行试验,以提高结果准确度。
平台型试剂盒适用于相近工艺产品线,可适用监测不同产品 HCP 水平。
目前通过Vero细胞培养的病毒有狂犬病病毒、脊髓灰质炎病毒等,种类繁多,工艺也各有千秋。湖州申科生物Vero细胞裂解型HCP残留检测试剂盒(一步酶联免疫吸附法)针对工艺过程中Vero细胞裂解后产生的大量不同种类的HCPs,可定量检测使用Vero细胞系生产并通过细胞裂解工艺收获的生物制品中宿主细胞蛋白的残留检测,抗体与校准品可覆盖近3000种蛋白。试剂盒操作简便,提高实验人员的时间利用率。试剂盒抗体覆盖率为65.1%-85.1%(IMBS-2D)和76.9%(IMBS-MS,Unique Peptide≥2)。试剂盒严格遵循ISO13485质量体系进行生产,并按照法规要求进行了性能验证,各项性能满足Vero宿主细胞蛋白检测需求。
SHENTEK® AutoElisa-4K HCP 检测自动化系统可减少人为误差,满足 21 CFR Part 11 数据管理要求。Sf9宿主细胞蛋白(HCP)残留检测抗体制备
抗体覆盖率是 HCP 检测关键指标,影响结果可信度,需通过方法验证。江苏宿主细胞蛋白(HCP)残留检测方法对比
湖州申科生物推出的宿主细胞残留蛋白检测全自动 ELISA 分析系统,整合了标曲制备、样本加样、恒温孵育、板孔清洗及结果检测等全流程功能。系统搭载的高精度前处理模块与检测模块,通准确控制实验参数,有效减少人为操作误差,确保实验结果的稳定性与准确性。其多模块单独运行设计,可实现不同检测任务的并行处理,大幅缩短实验周期,明显提升整体实验效率。在保障结果可靠的基础上,该系统实现了 ELISA 实验的自动化操作、标准化流程与快速化输出,降低了对实验人员的技能要求,同时通过优化资源配置减少检测成本。此外,系统内置完善的数据管理功能,可满足实验数据完整性记录与全流程审计追踪需求,严格符合 21 CFR Part 11 法规要求,并配备三级权限管理机制,进一步保障实验数据的安全性与规范性。
江苏宿主细胞蛋白(HCP)残留检测方法对比